
12 May CAPITULO 1 – EL CONCEPTO DE TEMPERATURA
Desde sus orígenes el ser humano fue capaz de distinguir entre el frío y el calor. Ello es así porque el desarrollo de la vida necesita unas condiciones ambientales bien determinadas, ni mucho frío ni demasiado calor.
Pero no es solamente el ser humano quien necesita de unas condiciones ambientales definidas, cualquier forma de vida, más aún, cualquier tipo de materia, necesita para su desarrollo unas condiciones ambientales adecuadas, entre las cuales se encuentra la temperatura.
El uso del vocablo temperatura evita controversias del tipo, “hay suficiente calor” contra “hay suficiente frío”, expresiones cuya ambigüedad técnica impide inclinarse por una u otra (sobre todo si se analizan fuera de contexto). Y es que en una escala de valores, calor y frío, representarían los dos extremos. ¿Podría llamarse a esa escala temperatura?
El uso del concepto de temperatura se complica algo cuando se utilizan los sentidos corporales para intentar fijar el punto de la escala de temperatura en que se encuentra un determinado objeto. Dicho de manera más simple, el ser humano es capaz por simple contacto (o sin él, como se verá más adelante) de establecer el nivel de temperatura de un objeto. Sin embargo a veces no resulta fácil. Por ejemplo, no se tiene la misma sensación de temperatura en los pies, cuando al salir de la cama se pisan las baldosas del suelo o la alfombra; la silla de madera o la metálica no parecen estar a la misma temperatura cuando se intentan coger, aunque ambas lleven tiempo inmersas en el mismo ambiente. La causa de estas diferencias en la evaluación de la temperatura es, que los sensores corporales captan el flujo calorífico que se intercambia entre el objeto y el cuerpo humano, de forma que el cerebro interpreta el sentido y la intensidad de este flujo, como una cantidad analógica de calor o frío. Que ello pueda ser una necesidad para proteger el cuerpo humano o exista o cualquier otra razón, no es objeto de esta exposición, en cualquier caso, quede constancia de esta singularidad.
Puede decirse que la temperatura es una propiedad de la materia que está directamente relacionada con su actividad molecular y que tiene un papel primordial en los procesos de intercambio energético. Debido a ello, la necesidad de conocer la temperatura de un proceso cualquiera es casi universal. Pero su determinación rigurosa no es fácil, como se verá más adelante.
Un poco de historia
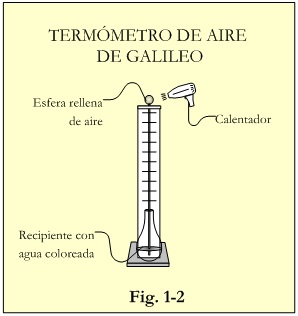
La medición de la temperatura forma parte del desarrollo científico de la humanidad casi desde sus orígenes. La civilización griega (Heron de Alejandría) ya dio muestras de su preocupación por el tema, posteriormente Filo de Bizancio hacia finales del siglo II realizó un manuscrito en el que se describen algunos experimentos. Más tarde, en 1638 Fludd realizó el termómetro de Filo, que estaba formado por una esfera hueca unida a un fino tubo, que estaban rellenos con un fluido acuoso coloreado. Colocando la esfera al sol, el aire contenido en su interior se calienta y expulsa parte del líquido contenido en el tubo. A continuación la esfera es llevada a la sombra y la contracción del aire provoca la entrada de agua en el tubo. Como se puede ver en la figura 1.1, se trata de un termómetro de gas muy elemental.

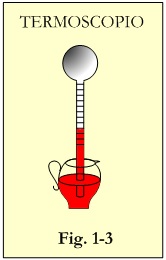
Se suele atribuir a Galileo la paternidad del termómetro hacia 1613. Se trataba de dispositivos no sellados, lo que hacía que la cantidad de aire atrapada dentro del termómetro fuese variable dando lugar a resultados poco fiables con baja calidad. Los primitivos instrumentos carecían de escala graduada y se denominan termoscopios. Las anotaciones se realizaban colocando un lazo de color en la zona del nivel de agua. La necesidad de comprobar la temperatura humana hizo que los físicos (médicos) adoptaran estos dispositivos, a los cuales les fué añadida posteriormente una escala graduada para facilitar su uso, naciendo así el termómetro. Normalmente se reconoce a Galeno como introductor de una escala de calor para el cuerpo humano; formada por ocho puntos, cuatro a cada lado de un punto central o neutro. Esta escala era frecuentemente incorporada en los termómetros del Renacimiento. Es probable que el primer punto fijo empleado para la graduación de los termómetros fuése la temperatura corporal.
Los constructores de termómetros eran especialistas con elevados conocimientos técnicos versados en astronomía y navegación. A pesar de ello, y debido al limitado estado de la tecnología, estos instrumentos proporcionaban mediciones muy poco reproductibles, existiendo grandes diferencias entre instrumentos, según su fabricante o la fecha de construcción.
Los termómetros de aire abiertos, eran influidos fuertemente por las variaciones de la presión atmosférica. Ello dio lugar a que algún tiempo después en 1654, Fernando II Gran Duque de Toscana propusiera mejorarlos por medio de una ejecución sellada y sustituir el aire por un líquido (alcohol etílico coloreado) como elemento dilatador. Claro que cualquier líquido dilata mucho menos que el aire, de modo que, para obtener una conveniente sensibilidad hubo de reducirse el diámetro interior del tubo de vidrio.
Con el paso del tiempo, los termómetros florentinos, así llamados por ser originarios de dicha República sus constructores, gozaron de un bien merecido prestigio por su calidad. Construidos con alcohol vinícola y vidrio, en diversas escalas (50, 100 y 300 divisiones), eran exportados a toda Europa. Figura 1.3.
En 1664, Robert Hook secretario de la Royal Society, usó alcohol tintado de rojo. Su escala, para la cual todos los grados presentaban igu al incremento de volumen equivalente a 1/500 parte del volumen del líquido del termómetro, necesitó solo un punto fijo. Para ello seleccionó el punto de congelación del agua, con el fin de fijar un criterio para obtener termómetros de diferentes tamaños con resultados iguales. El termómetro de Hook fué el estándar del Gresham College y fue usado por la Royal Society hasta 1709. (El primer registro meteorológico inteligible usó esta escala).
al incremento de volumen equivalente a 1/500 parte del volumen del líquido del termómetro, necesitó solo un punto fijo. Para ello seleccionó el punto de congelación del agua, con el fin de fijar un criterio para obtener termómetros de diferentes tamaños con resultados iguales. El termómetro de Hook fué el estándar del Gresham College y fue usado por la Royal Society hasta 1709. (El primer registro meteorológico inteligible usó esta escala).
En 1702, el astrónomo Ole Roemer de Copenhague basó su escala en dos puntos fijos: nieve (o hielo triturado) y el punto de ebullición del agua, y registró la temperatura diaria en Copenhague desde 1708 a 1709 con su termómetro.
El termómetro de Fahrenheit
En 1724 Gabriel Fahrenheit, un prestigioso fabricante alemán de termómetros, decidió utilizar mercurio como liquido termométrico. La expansión térmica del mercurio, amplia y suavemente uniforme, permite que no se adhiera al vidrio y permanece líquido en un amplio rango de temperaturas. Su aspecto plateado facilita la lectura. Fahrenheit calibró la escala de su termómetro de la siguiente manera:
«Colocando el termómetro en un mezcla de sal de amonio o agua salada, hielo y agua, determiné un punto sobre la escala que llamé cero. Un segundo punto obtenido de la misma manera, pero sin utilizar sal en la mezcla. Llamando a este punto 30. Un tercer punto designado como 96 se obtuvo colocando el termómetro en la boca para adquirir el calor del cuerpo humano.» (D.G Fahrenheit, Phil. Trans. (London) 33, 78, 1724).
Sobre esta escala, Fahrenheit midió el punto de ebullición del agua obteniendo 212 divisiones. Después el punto de congelación del agua, dando un resultado de 32, de forma que el intervalo entre el punto de congelación y ebullición del agua es de 180 divisiones. Las temperaturas medidas con esta escala son designadas como grados Fahrenheit (°F) ampliamente utilizados todavía en Estados Unidos de Norteamérica, a pesar de que este país está oficialmente acogido al Sistema Internacional (SI) cuyas unidades son el grado Celsius y el Kelvin.
La escala centígrada o Celsius
Hacia 1742 el astrónomo sueco Anders Celsius propuso la graduación centígrada, colocando el cero en el punto de ebullición del agua y el 100 en el hielo fundente. Posteriormente Marten Strömer invirtió ambos puntos quedando tal como se emplea actualmente. En la Conferencia Internacional de Temperatura de 1948 el término Grado Centígrado fue reemplazado por el de Grado Celsius.
Ambas unidades de medida se relacionan con la expresión:
ºC = 5/9 (ºF – 32)
Desarrollos posteriores
El físico francés J.A.C. Charles, en 1780, publicó un estudio según el cual, para un mismo incremento de temperatura, todos los gases presentan un aumento de volumen muy similar, de manera que los coeficientes de expansión de los gases están muy cerca unos del otros, y por ello es posible establecer una escala de temperatura basada en un solo punto fijo en vez de dos, tal como Fahrenheit o Celsius habían realizado las suyas. Esto condujo a la utilización de termómetros de gas como instrumento termométrico.
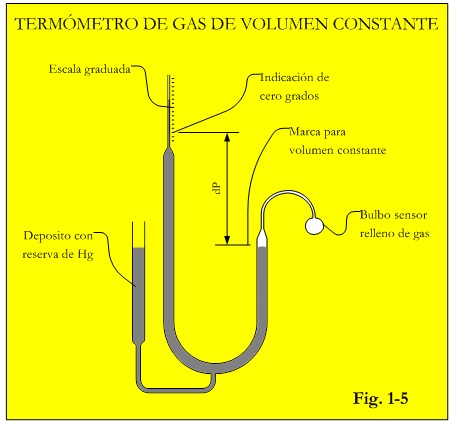
En el termómetro de gas a volumen constante (Figura 1-5) el bulbo sensor que contiene gas (por ejemplo hidrógeno) a una cierta presión, se conecta con un manómetro de mercurio por medio de un tubo de pequeño volumen (el bulbo es la parte sensible a la temperatura). El nivel de mercurio en el manómetro puede modificarse variando la altura del depósito. La presión del hidrógeno, que varía linealmente con la temperatura, es la diferencia entre los niveles “dP” más la presión exterior. Su linealidad para el rango entre 0 y 100ºC es bastante buena y la incertidumbre es de 0,002ºC
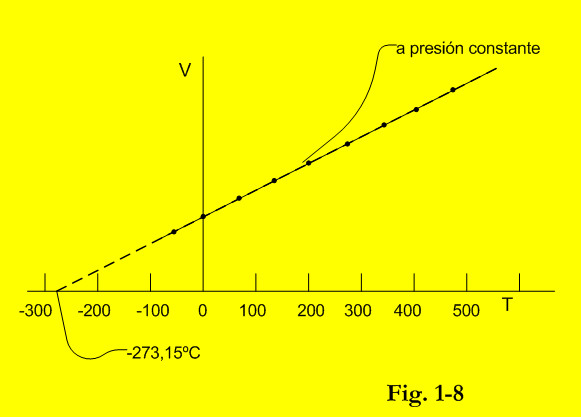
En el termómetro de gas a presión constante (Figura 1.6), la cámara de hidrógeno se ajusta a una presión constante por medio del pistón. En estas condiciones el volumen de gas de la cámara, indicado por la posición del pistón, es proporcional a la temperatura.
P. Chappuis in 1887 realizó extensos estudios sobre los termómetros de gas con presión constante o volumen constante, usando hidrógeno, nitróge-no y dióxido de carbono como medios termométricos. Basado en estos resultados, el Comité Interna-cional de Pesos y Medidas (CIPM) adoptó la escala de hidrógeno a volumen constante tomando como puntos fijos el punto de formación del hielo (0° C) y de vaporización (100° C) como escala práctica de temperatura.
Sir William Siemens en 1871 propuso un termómetro cuyo sensor es un conductor metálico que cambia su resistencia eléctrica con la temperatura. El platino no se oxida a altas temperaturas y presenta un cambio relativamente uniforme con la temperatura en un amplio rango. El termómetro de resistencia de platino (Fig. 1-7) es muy usado actualmente como termómetro de interpolación y cubre un rango de temperaturas desde -260° C hasta 1235° C.
T.J. Seebeck descubrió en 1826 que cuando son conectados entre si alambres metálicos de materiales distintos y ambas uniones se situan a diferentes temperaturas, fluye corriente que está relacionada cuantitativamente con la diferencia de temperaturas, de forma que el sistema conocido como termopar puede ser usado como termómetro. Es muy utilizado en la industria y se puede construir con diversas combinaciones de metales, como hierro / constantán, níquel / aluminio y platino / platino-rodio, entre otros.
Según Max Planck, temperatura es el grado de calor o frío de un cuerpo. Para R.H. Fowler, es que, dados tres cuerpos A, B y C, si A y C se encuentran en equilibrio térmico con B, entonces A y C también se encuentran en equilibrio térmico entre si. Esta definición es conocida como ley cero de la Termodinámica. En ciertos materiales puede decirse que es la medida de la densidad de calor de un cuerpo.
Realmente, no resulta sencillo expresar una definición clara de lo que es la temperatura, quizá porque dentro de cada individuo existe una noción intuitiva del fenómeno que representa, es posible enunciar muchas definiciones, todas válidas y probablemente todas incompletas. Ya se ha comentado anteriormente como trabajan los sentidos humanos para detectar el intercambio de calor con el exterior.
La temperatura puede considerarse como una medida del nivel de energía térmica. De forma análoga al concepto de tensión eléctrica con relación a la corriente, o a la altura en relación con la energía potencial. La temperatura es pues, la razón o fuerza generadora del flujo de calor.
Examinando la materia como conjunto de partículas microscópicas en un estado de agitación, la temperatura está relacionada con el numero de choques de estas partículas. Ello explica que cuando se comprime aire se produce un calentamiento del mismo. Es decir que la temperatura depende la energía cinética de las moléculas, la cual a su vez es función de la masa y velocidad de estas, además el numero de choques moleculares contra las paredes del recipiente que contiene el gas esta relacionado con la presión del mismo. De modo que, temperatura, presión, masa y volumen están directamente relacionados. Por otra parte temperatura y energía calorífica son conceptos interdependientes y dotados de la capacidad para realizar un trabajo.
Para expresar esta idea con más precisión, la temperatura puede tratarse como la energía promedio del movimiento de los átomos o moléculas que contiene una sustancia. Cuanto mayor sea la vibración o el movimiento de las partículas, más caliente estará dicha sustancia o lo que es lo mismo, mayor será su temperatura. Así mismo, algo más frío significa que sus partículas se mueven más lentas. La mínima temperatura alcanzable, llamada cero absoluto, se conseguirá cuando todas las partículas se detengan o se situen en un estado de máxima ordenación.
La ley de los gases ideales
En 1660, Robert Boyle demostró que para el aire contenido en un recipiente, se cumplía la relación P·V=constante, siendo P la presión y V el volumen del gas encerrado, a condición de mantener constante la temperatura del gas.
En 1787 Jacques Alexandre Charles estudió el comportamiento de los gases a presión constante, llegando a la conclusión de que el volumen ocupado por un gas está directamente relacionado con su temperatura, o dicho de otra forma que V/T=constante.
Más tarde en 1802 Joseph Louis Gay-Lussac reunió ambas conclusiones y extendió su alcance a otros gases como el oxígeno, nitrógeno, hidrógeno y dióxido de carbono. Realizó estudios sobre la dilatación los gases y determinó que el volumen a t grados centígrados viene dado por la expresión:
donde α es el coeficiente de dilatación, cuyo valor era de 1/267.
Posteriormente en 1847, Victor Regnault realizo una determinación más exacta y obtuvo el valor de 1/273.
Con el desarrollo de la teoría cinética a mediados del siglo XIX, nace el concepto de gas ideal, cuyo comportamiento al aplicarle las leyes de la mecánica de Newton, coincide sensiblemente con el de los gases reales diluidos. Se comprueba que el coeficiente de dilatación de los gases es muy similar para todos ellos y vale α=1/273,15 para un intervalo de temperatura comprendido entre los puntos de congelación y vaporización del agua.
Utilizando la expresión [1.1] para determinar la temperatura a la cual el volumen se hace mínimo:
Así pues, parece que para los gases perfectos (o reales diluidos) la mínima temperatura posible es de -273,15, aunque en la realidad sucede que el gas se licua antes.
La relación entre P (presión), V (volumen) y T (temperatura) para los gases perfectos quedo finalmente enunciada como:
donde T es la temperatura absoluta (es decir, asignando el valor de cero al mínimo valor posible), R es la constante universal de los gases (8,314 J·mol-1·K-1) cuando estos se encuentran a muy baja presión (esta condición es necesaria para que el comportamiento de los gases reales sea semejante a los ideales) y n es el número de moles.
Este concepto del cero absoluto de temperatura es muy importante, puesto que viene a decir que la energía térmica de un sistema se va reduciendo a medida que la temperatura se aproxima a éste valor. En el cero absoluto no existiría energía térmica y solamente quedaría la energía de enlace.
Medición de temperaturas
La ley de los gases perfectos y su conclusión sobre la temperatura absoluta, dio origen a los trabajos para construir termómetros capaces de determinar la temperatura de forma rigurosa. Particularmente en el campo de la medición de temperatura del aire por meteorólogos y astrónomos. Los termómetros de gas iniciaron su desarrollo. El método de medición de bajas temperaturas por medio de gases ligeros a muy baja presión fué adoptado por la mayor parte de los científicos, dado que ese método permitía la determinación de la temperatura sobre bases rigurosamente termodinámicas. Las figuras 1‑5 y 1-6 representan de forma esquematizada dispositivos de este tipo, cuya respuesta vendría a ser la figura 1-8.
Los estudios termodinámicos de Sadi Carnot sobre máquinas térmicas, mostraron que la eficiencia máxima se consigue cuando el ciclo de trabajo es realizado por medio de procesos reversibles, expansión isotérmica/adiabática y compresión isotérmica/adiabática, dependiendo solo de la temperatura. Concretamente, la relación entre calor cedido y tomado es igual al cociente de las temperaturas de los focos frío y caliente, que puede ser expresado así:
Lord Kelvin comprobó la íntima relación existente entre la ley de los gases perfectos [1.2] y el teorema de Carnot [1.3], demostrando la naturaleza termodinámica de la temperatura, aunque desgraciadamente no proporcionó demasiadas pistas sobre su naturaleza. Más tarde los trabajos de diversos físicos, entre los que cabe señalar a Maxwell, Boltzmann y Gibb, sobre la mecánica estadística y los movimientos y colisiones de los átomos individuales en un recinto cerrado, mostraron que el equilibrio térmico se alcanza cuando la energía cinética media es la misma para todos los átomos. Resultando la expresión:
en la que el término m·v2/2 es la energía cinética promedio que anima a cada átomo del gas. Si se comparan las expresiónes [1.2] y [1.4] se puede concluir que la temperatura termodinámica (o absoluta) es proporcional a la energía cinética promedio del átomo. Cuando se trata de gases moleculares la energía cinética total es mayor que en los gases monoatómicos debido a que además de vibrar pueden rotar; en este caso la temperatura es proporcional a la energía cinética media de traslación.
Cuando se aplican los principios de la Termodinámica y la Mecánica Estadística a otros sistemas se pueden obtener otros métodos para la determinación de las temperaturas termodinámicas. Así se tienen las cuatro relaciones siguientes:
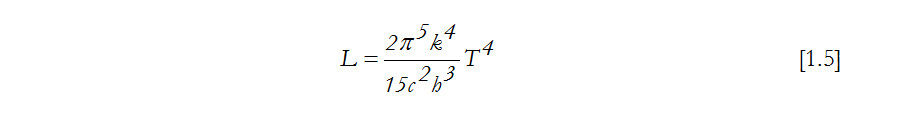
Que da la radiación total L en función de la temperatura. Siendo k, c y h las constantes de Boltzmann, velocidad de la luz y Planck respectivamente.
Esta expresión relaciona la radiación espectral Lλ en función de la longitud de onda, λ del índice de refracción n y de la temperatura T.
Relación entre la velocidad del sonido cs y el calor específico γ, masa molecular m y temperatura T.
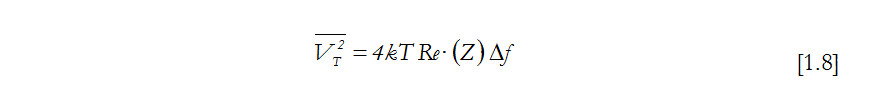
Según la cual la temperatura es función del ruido en una resistencia eléctrica. Siendo ![]() la tensión media cuadrática, Z la parte real de la impedancia y Δf la anchura de banda.
la tensión media cuadrática, Z la parte real de la impedancia y Δf la anchura de banda.
Todas ellas permiten construir termómetros para la medición de la temperatura termodinámica. Sin embargo la precisión obtenida o la repetibilidad de las medidas deja bastante que desear, cuando se trata de obtener elevada precisión.




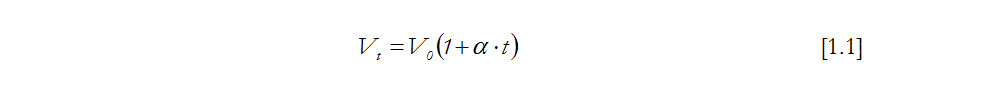
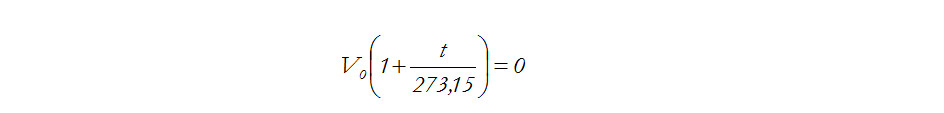
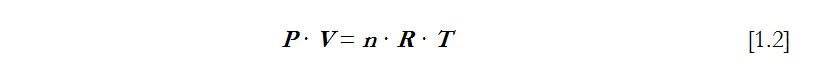
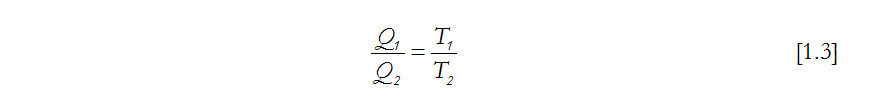
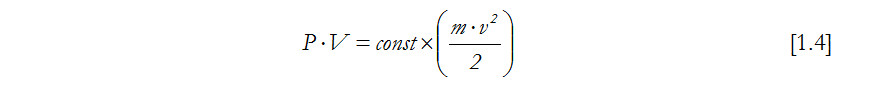
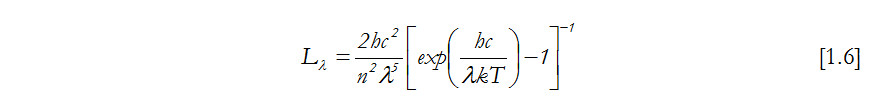
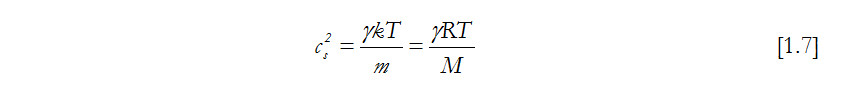
Sorry, the comment form is closed at this time.